 W
WOddychanie komórkowe – wielostopniowy biochemiczny proces utleniania związków organicznych związany z wydzieleniem energii użytecznej metabolicznie. Oddychanie przebiega w każdej żywej komórce w sposób stały. Zachodzi ono nawet wtedy, gdy inne procesy metaboliczne zostaną zahamowane. Chociaż istnieją różnice w przebiegu procesu oddychania u poszczególnych grup organizmów, to zestaw enzymów katalizujących poszczególne reakcje składające się na oddychanie jest zbliżony u wszystkich organizmów żywych. Zachodzenie oddychania jest jednym z najczęściej stosowanych wskaźników zachodzenia procesów życiowych. Jedynie wirusy będące strukturami na pograniczu życia i cząstek chemicznych nie przeprowadzają procesu oddychania.
 W
WAdenozyno-5′-trifosforan, ATP, daw. adenozynotrójfosforan – organiczny związek chemiczny, nukleotyd adeninowy zbudowany z adenozyny z przyłączoną wiązaniem estrowym w pozycji 5′-OH grupą trifosforanową. Odgrywa on ważną rolę w biologii komórki jako wielofunkcyjny koenzym i molekularna jednostka w wewnątrzkomórkowym transporcie energii. Stanowi nośnik energii chemicznej, używanej w metabolizmie komórki. Powstaje jako magazyn energii w procesach fotosyntezy i oddychania komórkowego. Zużywają go liczne enzymy, a zgromadzona w nim energia służy do przeprowadzania różnorodnych procesów, jak biosyntezy, ruchu i podziału komórki. Tworzy się z adenozyno-5′-difosforanu, a przekazując swą energię dalej, powraca do formy ADP lub adenozyno-5′-monofosforanu (AMP). Cykl ten zachodzi bezustannie w organizmach żywych. Człowiek dorosły w ciągu doby syntetyzuje i zużywa około 85 kg adenozynotrifosforanu (ATP).
 W
WAnaerob fakultatywny, względny beztlenowiec – typ organizmu anaerobowego, zwykle bakterii, który rośnie zarówno w środowisku zawierającym tlen, jak i pozbawionym tlenu. Wyróżniane są dwa typy względnych beztlenowców. Pierwszy to organizmy, które rozwijają się w obecności tlenu, wytwarzając energię metaboliczną przez fermentację, i nie korzystają z tlenu w swoim metabolizmie; takie organizmy nazywane są aerotolerancyjnymi. Druga grupa w zależności od dostępu tlenu pozyskuje energię dzięki oddychaniu tlenowemu lub fermentacji, w zależności od warunków, w jakich się znajduje.
 W
WCentra żelazowo-siarkowe, centra żelazo-siarkowe – to grupy prostetyczne wielu enzymów. Występują one w białkach wszystkich żywych organizmów, między innymi w niektórych enzymach mitochondrialnego łańcucha oddechowego i są niezbędne do życia komórki. Centra żelazo-siarkowe znajdują się w białkach z tak zwanym żelazem niehemowym. Znanych jest kilka rodzajów centrów żelazo-siarkowych. Najprostsze z nich zawiera jeden jon żelaza połączony z czterema resztami cysteiny. Drugi rodzaj określany 2Fe-2S składa się z dwóch jonów żelaza połączanych dwoma atomami siarki nieorganicznej. Jednocześnie każdy z jonów żelaza koordynowany jest zwykle dwoma resztami cysteiny. Trzeci rodzaj centrów 4Fe-4S składa się z czterech jonów żelaza i czterech atomów siarki nieorganicznej połączonych w kształt sześcianu. Ten rodzaj centrów występuje w białku Rieske.
 W
WChemiosmoza – proces biochemiczny polegający na przemieszczaniu protonów przez błony białkowo-lipidowe z wytworzeniem ATP. Pojęcie to wprowadził Peter D. Mitchell tłumacząc powstawanie ATP w mitochondriach, polegające na zamianie energii zgromadzonej w postaci gradientu elektrochemicznego na energię wiązań ATP. W toku dalszych badań wykazano, że ATP wytwarzane jest przez syntazę ATP wykorzystującą energię gradientu elektrochemicznego.
 W
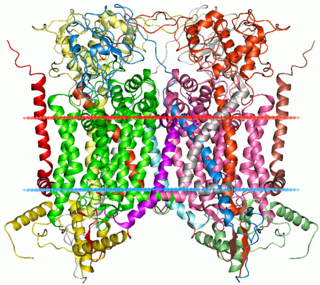
WCykl Q – seria reakcji biochemicznych, których przebieg jako pierwszy opisał Peter D. Mitchell w 1977 roku. Kolejne reakcje utleniania i redukcji przenośnika elektronów znajdującego się w błonach białkowo-lipidowych, ubichinonu, prowadzą do przenoszenia protonów przez dwuwarstwę lipidową. Zmodyfikowana wersja schematu zaproponowanego przez Mitchella tłumaczy w jaki sposób kompleks III obecny w błonie mitochondrialnej przenosi protony z macierzy mitochondrialnej (matrix) do przestrzeni międzybłonowej (perymitochondrialnej).
 W
WCytochrom b/b6 – główna podjednostka transbłonowych kompleksów cytochromów bc1 i b6f.
 W
WOksydoreduktaza Q – cytochrom c, inaczej cytochrom bc1, kompleks III, kompleks oksydoreduktazy ubichinon-cytochrom c – białko błonowe łańcucha oddechowego, zlokalizowane w wewnętrznej błonie mitochondrialnej, o masie 250 kDa i zbudowane z 10 podjednostek. Zawiera grupy prostetyczne takie, jak hem bH, hem bL, hem c1 oraz Fe-S.
 W
WCytochrom c – hemoproteina pełniąca funkcję transportera elektronów w łańcuchu oddechowym pomiędzy kompleksem cytochromów bc1 a oksydazą cytochromową w mitochondriach. Rodzina cytochromów c jest jedną z najlepiej scharakteryzowanych rodzin białek.
 W
WDehydrogenaza bursztynianowa – enzym z grupy oksydoreduktaz katalizujący reakcje odwodornienia bursztynianu z wytworzeniem fumaranu. W grupie prostetycznej enzymu występuje FAD. Na każdą grupę flawinową przypadają 4 atomy żelaza i 4 jony siarczkowe. Dehydrogenaza bursztynianowa u eukariontów jest zlokalizowana w wewnętrznej błonie mitochondrium. Jest to jedyny z enzymów Cyklu Krebsa związany z wewnętrzną błoną mitochondrialną. Jej inhibitorem kompetycyjnym jest np. malonian.
 W
WDehydrogenaza NADH, oksydoreduktaza NADH-ubichinon, kompleks I łańcucha oddechowego (EC 1.6.5.3) – jest to enzym obecny w wewnętrznej błonie mitochondrów eukariotów oraz błonach komórkowych prokariotów. Rozpoczyna szereg reakcji określanych jako łańcuch oddechowy poprzez utlenianie NADH przy jednoczesnej redukcji ubichinonu obecnego w błonie. Przeniesieniu dwóch elektronów pobranych z NADH na ubichinon prowadzi do powstania ubichinolu, jednocześnie cztery protony przez kompleks przenoszone są na zewnętrzną stronę błony białkowo-lipidowej.NADH + H+ + CoQ + 4H+wew. → NAD+ + CoQH2 + 4H+zew.
 W
WFosforylacja oksydacyjna – szlak metaboliczny, w którego wyniku energia, uwalniana podczas utleniania zredukowanych nukleotydów, przekształcana jest w energię ATP. Organizmy żywe wykorzystują wiele różnych związków organicznych, jednak aby wytworzyć z nich energię przydatną metabolicznie, cząsteczki ATP, w większości przeprowadzają fosforylację oksydacyjną. Szlak ten jest dominujący ze względu na wysoką efektywność w porównaniu do alternatywnych sposobów syntezy ATP, czyli fermentacji.
 W
WGlikoliza, szlak Embdena-Meyerhofa-Parnasa – ciąg reakcji biochemicznych, podczas których jedna cząsteczka glukozy zostaje przekształcona w dwie cząsteczki pirogronianu.
 W
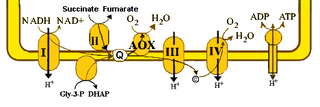
WOksydaza alternatywna (AOX z ang. alternative oxidase) – enzym obecny w wewnętrznej błonie mitochondriów roślin, glonów, grzybów i niektórych protistów. Geny kodujące AOX zostały zidentyfikowane również u przedstawicieli proteobakterii oraz zwierząt bezkręgowych należących do strunowców, półstrunowców, szkarłupni, nicieni, mięczaków, pierścienic, parzydełkowców czy gąbek. Enzym ten stwarza alternatywną możliwość przenoszenia elektronów z ubichinonu na tlen. Podczas klasycznego łańcucha oddechowego elektrony pobierane z NADH przekazywane są na ubichinon, a następnie poprzez kompleks cytochromowy bc1 i cytochrom c na oksydazę cytochromową. Oksydaza alternatywna przenosi elektrony na tlen z pominięciem kompleksu III i kompleksu IV łańcucha oddechowego. W efekcie jej działania NADH lub FADH2 zostają utlenione z wytworzeniem H2O jednak gradient elektrochemiczny nie powstaje a tym samym energia zgromadzona utlenianych NADH i FADH2 nie jest zamieniana na ATP lecz uwalniana w postaci ciepła. Szczególna cechą oksydazy alternatywnej jest jej niewrażliwość na inhibitory oksydazy cytochromowej np. cyjanek, siarkowodór, azydek, tlenek węgla oraz tlenek azotu. W tkankach zwierzęcych podanie 1 mmol l-1 KCN powoduje całkowite zatrzymanie oddychania komórkowego, w tkankach roślinnych oddychanie komórkowe zmniejsza się do poziomu 10-20% oddychania przed podaniem inhibitora. Zachodzące z udziałem oksydazy alternatywnej oddychanie komórkowe określa się jako alternatywną drogę oddechową lub oddychanie niewrażliwe na cyjanek.
 W
WOksydaza cytochromu c (też oksydaza cytochromowa, kompleks IV łańcucha oddechowego) – to duży transbłonowy kompleks białkowy błony wewnętrznej mitochondrium oraz bakterii. Jest to ostatnie białko łańcucha oddechowego (IV). Odbiera elektrony (utlenia) z cytochromów c i przenosi je na cząsteczkę tlenu, redukując go, wskutek czego po przyłączeniu jonów H+ powstają dwie cząsteczki wody. Podczas tego procesu, przenosi także przez błonę cztery jony H+, wspomagając powstawanie potencjału chemiosmotycznego.
 W
WSyntaza ATP, – enzym z grupy syntaz katalizujący reakcję wytwarzania ATP z ADP i fosforanu nieorganicznego Pi. Energia niezbędna do syntezy pochodzi z gradientu elektrochemicznego protonów - w wyniku tego gradientu następuje ruch protonów, a następnie ich energia przekształcana jest w energię wiązań chemicznych w ATP.
 W
WSzlak Entnera-Doudoroffa – szereg reakcji biochemicznych prowadzący do przekształcenia cząsteczki glukozy do dwóch cząsteczek pirogronianu. Jest to szlak alternatywny do glikolizy. W wyniku takiego przekształcenia powstaje po jednej cząsteczce ATP, NADH i NADPH. Dla porównania, w glikolizie zyskiem netto przekształcenia cząsteczki glukozy są po dwie cząsteczki ATP i NADH.
 W
WUbichinon, koenzym Q10 – organiczny związek chemiczny z grupy chinonów, występujący w mitochondriach komórek roślinnych i zwierzęcych. Jest odpowiedzialny za przenoszenie elektronów w łańcuchu oddechowym. Po przyłączeniu elektronów swobodnie porusza się w wewnętrznej błonie mitochondrialnej umożliwiając transport elektronów między kompleksami białek łańcucha oddechowego, które wbudowane są w wewnętrzną błonę mitochondrialną. Przenosi elektrony między dehydrogenazą NADH (kompleks I), względnie reduktazą bursztynian-koenzym-Q (kompleks II) na kompleks cytochromów bc1, jest więc miejscem zejścia się dróg elektronów pochodzących z NADH oraz FADH2.
 W
WUrydyno-5′-trifosforan (UTP) – organiczny związek chemiczny, rybonukleotyd pirymidynowy pełniący funkcję przenośnika energii w komórce. Pełni on podobne funkcje do adenozynotrifosforanu (ATP), tj. bierze udział w reakcjach fosforylacji, a także dostarcza energię w procesie transkrypcji oraz translacji. Podobnie jak ATP, urydynotrifosforan zawiera dwa wysokoenergetyczne wiązania fosforanowe.